Bron 04-10-2025, 20:21 Wat weten we nu over het intestinale microbioom? – MediQuality
Op het 59e congres van de AMUB begin september 2025 in Brussel (AMUB 2025) is een
presentatie gehouden over het intestinale microbioom.
De presentatie is gegeven door Louison Toris van het laboratorium voor experimentele
gastro-enterologie aan de ULV en coauteur van een artikel over dat onderwerp in de
Revue médicale de Bruxelles
Het onzichtbare wordt meetbaar
De spreekster heeft er eerst aan herinnerd dat het onderzoek van het microbioom pas echt
van start is gegaan in de jaren 2000 dankzij de ontwikkeling van sequencingtechnieken
met een hoog debiet (waarvan de kosten vervolgens sterk zijn gedaald). Het jaar 2007 is
een keerpunt geweest met de lancering van het Human Microbiome Project (HMP). Louison
Toris vat die evolutie als volgt samen: “We leven in een tijd dat het onzichtbare meetbaar
wordt”.
Evolutie van het aantal publicaties over het microbioom
Het microbioom is essentieel voor de gezondheid. Microbiota komen voor op tal van
plaatsen: huid, mond, urogenitale tractus, luchtwegen, maar toch vooral in de darmen. Het
intestinale microbioom is goed voor 70% van het totale microbioom bij de mens. Het
bestaat vooral uit bacteriën (99%), maar bevat ook virussen (0,1-1%), archaea (< 1%),
schimmels (0,01-0,1%) en parasieten.
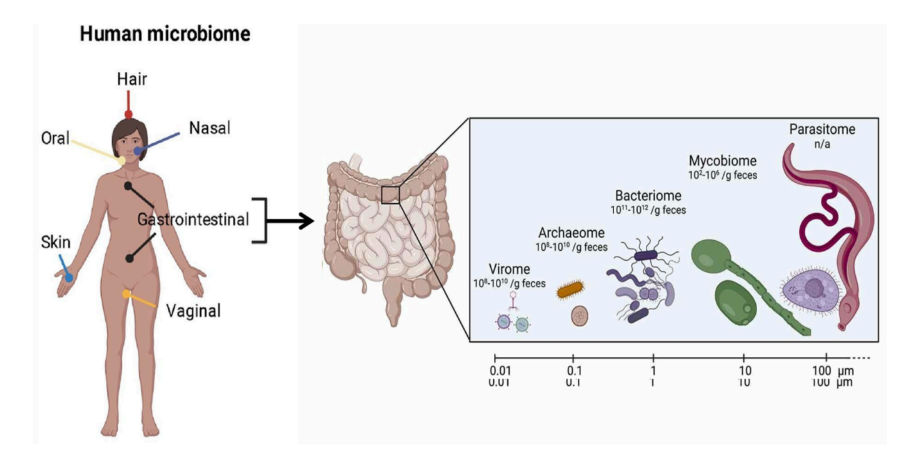
Ieder individu heeft een uniek microbioom
Het intestinale microbioom verschilt van de ene mens tot de andere. Het heeft meerdere
essentiële functies waaronder: gisting van niet-verteerbare voedingsvezels, waarbij vooral
korteketenvetzuren worden gevormd, synthese van vitamines (vitamine K en de meeste
wateroplosbare vitamines van de B-groep), productie van aminozuren, preventie van
kolonisatie van het spijsverteringskanaal door pathogene kiemen en actieve participatie
aan de rijping van het immuunsysteem. Vanaf de geboorte stimuleert het microbioom
receptoren die moleculaire motieven herkennen (PPR > TLR), en produceert het
antimicrobiële peptiden, IgA en pro-inflammatoire cytokines, die immuuncellen rekruteren.
De eerste 3 levensjaren
Uit studies bij tweelingen is gebleken dat genetica weinig invloed heeft op het intestinale
microbioom, dat vooral wordt bepaald door de omgeving. De eerste 3 levensjaren zijn
beslissend wat dat betreft. Belangrijke factoren zijn de wijze van geboorte (via natuurlijke
weg of via een keizersnede) en het type voeding. Daarna volgt het exposoom: voeding,
inname van antibiotica, sportactiviteit, stress, circadiaanse ritmes ….
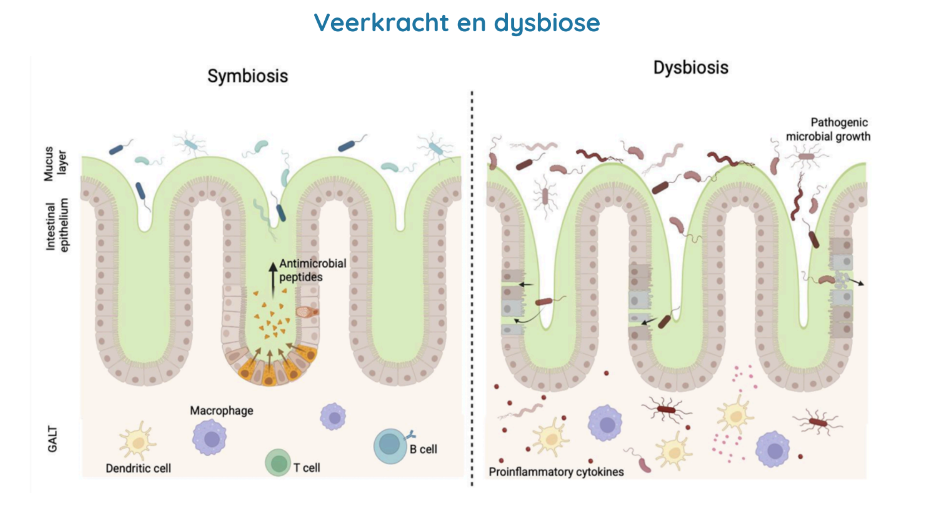
Een dynamisch en veerkrachtig systeem
Een van de kenmerken van het intestinale microbioom is zijn veerkracht. Na agressie slaagt
het er doorgaans in toch weer normaal te gaan functioneren … maar het mag niet te gortig
worden. Bij langdurige of chronische druk (herhaalde infecties, onevenwichtige voeding,
chronische stress ….) blijft het evenwicht in het intestinale microbioom ontwricht en ontstaat
een toestand van dysbiose. Dysbiose, een verlies van homeostase, werkt de
vermenigvuldiging van opportunistische bacteriën in de hand, vermindert de productie van
slijm, dat de darmwand beschermt, en leidt tot ontsteking. Dat kan leiden tot allerhande
ziektes van het spijsverteringsstelsel (chronische inflammatoire darmaandoeningen ….),
metabole (obesitas ….) en neuropsychiatrische aandoeningen.
Aanwezigheid ≠ activiteit
De laatste jaren is duidelijk geworden dat de aanwezigheid van een bacterie in de darmen
daarom nog niet betekent dat ze actief is. Met de huidige technieken kunnen we de rol en
de activiteit van de componenten van het microbioom beter exploreren.
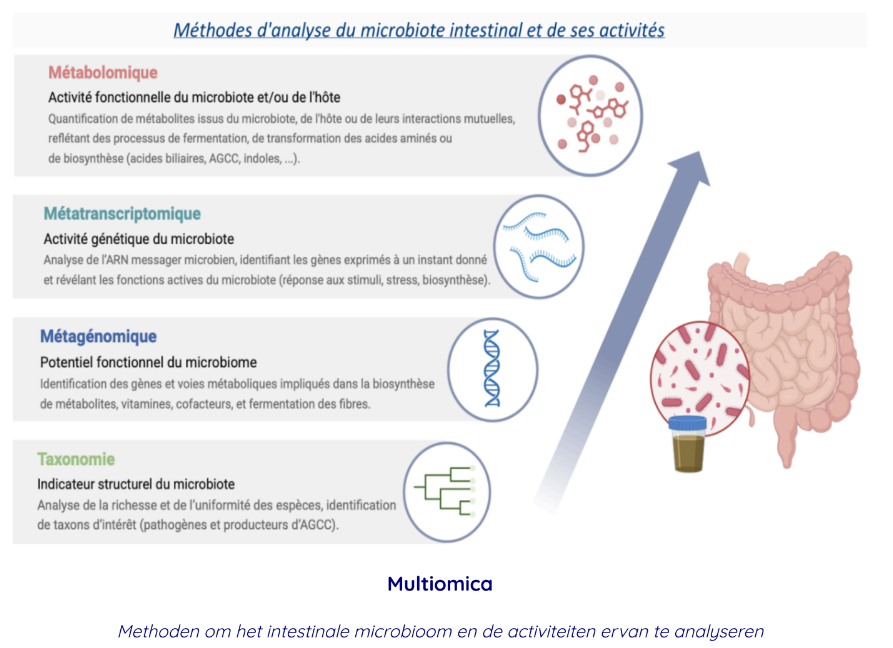
Metabolomica
Functionele activiteit van het microbioom en/of de gastheer
Meting van metabolieten van het microbioom, de gastheer of hun onderlinge
interacties als gevolg van gisting, transformatie van aminozuren of biosynthese
(galzuren, korteketenvetzuren, indolderivaten …)
Metatranscriptomica
Genetische activiteit van het microbioom
Analyse van het microbiële mRNA met identificatie van genen die op een gegeven
ogenblik tot expressie worden gebracht en te maken hebben met de actieve functies
van het microbioom (respons op prikkels, stress, biosynthese).
Metagenomica
Functioneel potentieel van het microbioom
– Identificatie van genen en metabole wegen die meespelen bij de biosynthese van
metabolieten, vitamines, cofactoren en fermentatie van vezels.
Taxonomie
Structurele indicator van het microbioom
– Analyse van de rijkheid aan en de uniformiteit van de species, identificatie van
specifieke taxonen (pathogenen en bacteriën die korteketenvetzuren produceren).
Een van de bekendste klinische toepassingen is waarschijnlijk transplantatie van fecale
microbiota, die bijzonder effectief is bij een recidiverende Clostridium difficile-infectie, een
monofactoriële ziekte.
Bij multifactoriële aandoeningen is het gecompliceerder. Dat is net hét probleem bij gebruik
van pre- en probiotica, die nochtans zeer populair zijn.
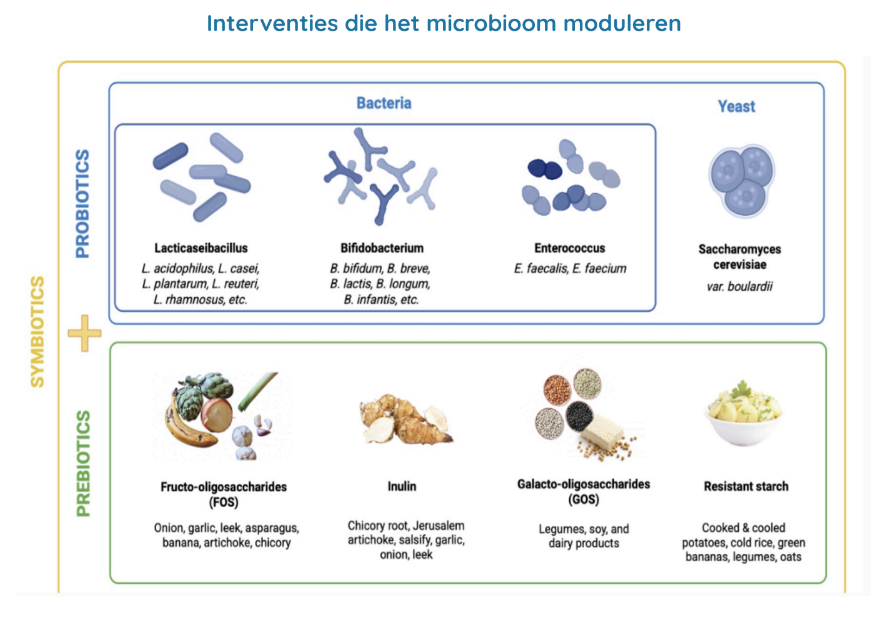
Wat is een gezond intestinaal microbioom?
De vele studies die de werkzaamheid hebben onderzocht van interventies die het
intestinale microbioom moduleren, hebben zeer uiteenlopende resultaten voortgebracht.
De belangrijkste obstakels zijn de hoge variabiliteit van de ene mens tot de andere en het
ontbreken van een duidelijke definitie van een “gezond” microbioom.
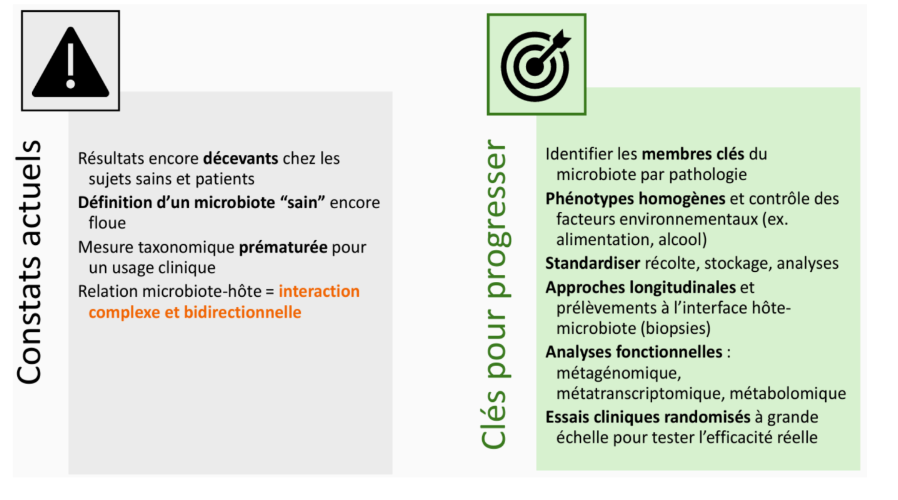
Huidige vaststellingen
Resultaten bij gezonde mensen en patiënten nog ontgoochelend
Nog geen alom aanvaarde definitie van een “gezond” microbioom
Taxonomische meting prematuur voor klinisch gebruik
Relatie microbiota-gastheer = complexe en bidirectionele interactie
Sleutels tot vooruitgang
Identificatie van de belangrijkste microbiota per pathologie
Homogene fenotypes en controle van de omgevingsfactoren (bv. voeding, alcohol)
De afname, bewaring en analyses standaardiseren
Longitudinale analyses en afnames van de interface tussen gastheer en microbiota
(biopsies)
Functionele analyses: metagenomica, metatranscriptomica, metabolomica
Grootschalige gerandomiseerde, gecontroleerde studies om de werkzaamheid te
evalueren
We weten nog niet welk probioticum in welke indicatie geïndiceerd is bij welke patiënt, maar
het onderzoek gaat met rasse schreden vooruit. Binnenkort zullen we meer weten.
Bronnen:
- Louison Toris, Center for the Study of IBD, Laboratoire de gastroentérologie
expérimentale, Université libre de Bruxelles (ULB), État de l’art sur le microbiote
intestinal en 2025 et implications cliniques, 59 Congrès de l’AMUB, sept. 2025,
Bruxelles. https://www.amub-ulb.be/evenement/59e-congres-de-l-amub. Contenu
accessible dans l’espace membre.
- TORIS L. et LIEFFERINCKX C., State of the art on the gut microbiota in 2025 and clinical
implications, Revue médicale de Bruxelles. Volume 45 n 4, sept. https://www.amub-ulb.be/revue-medicale-bruxelles/article/etat-de-l-art-sur-le-microbiote-intestinal-en-2025-et-implications
